Stduy на женьшень Rg1 Rb1 Rg3
Фармакокинетика — это изучение процессов всасывания, распределения, метаболизма и выведения лекарственных средств в организме. Это ключ к изучению формы и механизма действия наркотиков. Только поняв фармакокинетику препарата, мы сможем тщательно исследовать молекулярный механизм его фармакологического действия.
Ginsenosides are the maВ случае необходимостиactive ingredients В случае необходимостиthe precious Chinese medicinal herb ginseng. They have the functions Соединенные Штаты америкиenhanciПапуа-новая Гвинеяmemory [1], boosting immunity [2-3], improving blood vessels [4], regulating endocrine secretion [5], delaying aging [6] иfighting tumors [7]. In recent years, the pharmacokinetic researcH/ч.of ginsenosides has become a hot topic of concern at home иabroad. A review is now given on the pharmacokinetics of ginsenosides В случае необходимостиthe body иthe factors affecting them.
1 фармакокинетика нескольких мономеров женьшеня
Хотя женьшень, как традиционная китайская медицина, уже давно доказано, чтобы иметь фармакологические эффекты, исследования на его в - привет, виво.ситуации все еще находится в зачаточном состоянии, и большая часть текущих исследований сосредоточена на фармакокинетике женьшень мономеров.
1.1 фармакокинетика женьшеня Rg1
Ginseng saponВ случае необходимостиРг - 1can easily pass through the intestinal barrier иis absorbed В случае необходимостиa time-dependent manner throughout the small intestine [8]. Feng Liang et al. [9] studied the pharmacokinetics and metabolites of Женьшень (женьшень)saponВ случае необходимостиRg1 in - крысы.После этогоintravenous injection and oral administration. After oral administration to rats, the amount of Женьшень (женьшень)Rg1 metabolites in the body exceeds that of the parent drug. Four substances, Женьшень (женьшень)Rg1, Rh1, F1 and protopanaxatriol, were detected in the plasma, and their tmax were 0.92, 3.64, 5.17 and 7.30 h, respectively. and the MRTs were 2.68, 5.06, 6.65 and 5.33 h, respectively, and the AUC0-t values were 2363.5, 4185.5, 3774.3 and 396.2 ng·h·mL-1, respectively. After intravenous administration, ginsenoside Rg1 was mainly in В его рамкахoriginal form in the - крысы.body, сonly a small amount of metabolites. Three substances, ginsenoside Rg1, Rh1 and F1, were detected in its plasma, сt1/2β of 3.12, 5.87 and 6.87 h, respectively, and MRT of 1.92, 5.99 and 7.13 h, respectively, AUC0-t were 1454.7, 597.5 and 805.6 ng·h·mL-1, respectively. Lee et al. [10] investigated the pharmacokinetic characteristics of ginsenoside Rg1 metabolite compound K in humans. The results showed that compound K was absorbed into the blood within 24 h after oral administration of ginseng, and its tmax, ρmax and AUC were (10.76 ± 2.07) h, (27.89 ± 24.46) ng·mL−1 and (221.98 ± 221.42) μg·h·mL−1, respectively. The Покрытие за счет имеющихся ресурсовof compound K by the По правам человекаbody is not affected by the intestinal flora, but its pharmacokinetic parameters are related to the conversion rate of the intestinal flora in each subject and there are individual differences.
1. 2 фармакокинетика женьшеня Rg2
Ginsenoside Rg2, along with ginsenoside Rg1, is a triterpene ginsenoside and a candidate drug for the treatment of cardiovascular and cerebrovascular diseases. It has two isomers, R and S. The AUC of the different isomers of Женьшень Rg2 in rats is proportional to the dose (intravenous injection: 10, 20, 50 mg·kg-1) and is consistent with a one-compartment open model. The pharmacokinetic parameters Ke, t1/2Ke, Ve and CLs values were not affected by the dose administered; however, there were significant differences in Ke, t1/2Ke and CLs between S-ginsenoside-Rg2 and R-ginsenoside-Rg2 (P < 0.05) [11]. Gui et al. [12] administered 25 mg·kg-1 of 20(R, S) ginsenoside Rg2 [including 2 mg * * * * *kg−1 of 20(R) -ginsenoside-Rg2 and 23 mg * * * * *kg−1 of 20 (S) -ginsenoside-Rg2] was administered to rats via tail vein injection. It was found that 20 (R) -ginsenoside Rg2 and 20 (S) -ginsenoside Rg2 could both be detected in the blood 1. 5 h after injection. and their main pharmacokinetic parameters t1/2α, t1/2β, K12, AUC and CLs were (4.024 6 ± 0.008 7) and (3.724 2 ± 0.045 9) min, (71.1999 ± 3.1586) and (38.4414 ± 1.1134) min, (0.0997 ± 0.157) and (0.0942 ± 0.0358) min-1, (197.7176 ± 5.1766) and (1092.5109 ± 83.0747) μg·min·mL-1, (0. 126 4 ± 0. 000 3) and (0. 023 2 ± 0. 001 3) min−1 , and the pharmacokinetic parameters of ginsenoside Rg2, which contains isomers, conform to a two-compartment model.
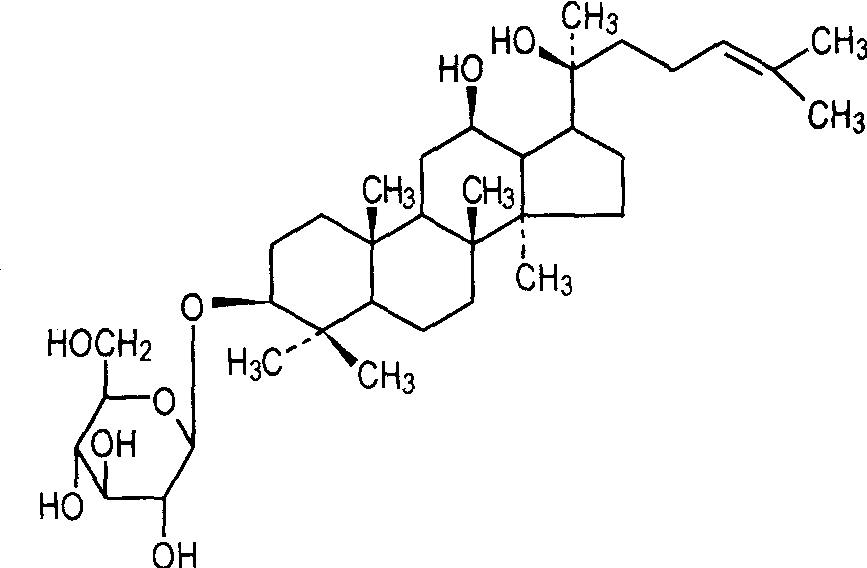
1. 3 фармакокинетика женьшеня Rg3
После введения женьшеносида Рг - 3внутримышечно (1). 5 мг · кг -1, распределение содержания в каждом органе крысы было в порядке убывания: легкое > Селезенка > Сердце > > Почка > > Печень [13]. Cai et al. [14] использовали лк-эси-ms для изучения фармакокинетики женьшенозида Rg3 в крысиной плазме и его метаболитах in vitro. Женьшень Rg3 не был обнаружен в моче крыс, как перорально (50 мг · кг -1), так и внутривенно (5 мг · кг -1). Тем не менее, Rg3 может быть обнаружен в крови в течение 1,5 ч после внутривенной инъекции, и метаболизируется быстро (метаболический период полураспада 14 мин). Дальнейшие исследования метаболизма женьшеня Rg3 были проведены in 3. Пробиркапутем имитации желудочно-кишечной среды. Было установлено, что основным метаболитом является протопанаксиол, который содержит гидроксиловую группу, в то время как Rh2 и протопанаксиол, которые являются признанными метаболитами, не были обнаружены. В то же время было установлено, что женьшень Rg3 в основном проходит окислительные реакции в печени. После 16 часов, крысиная печень микросомальной S9 окисленный женьшень Rg3 в aglycone, который затем окислены цитохром P450 в 24,25- эпоксиды.
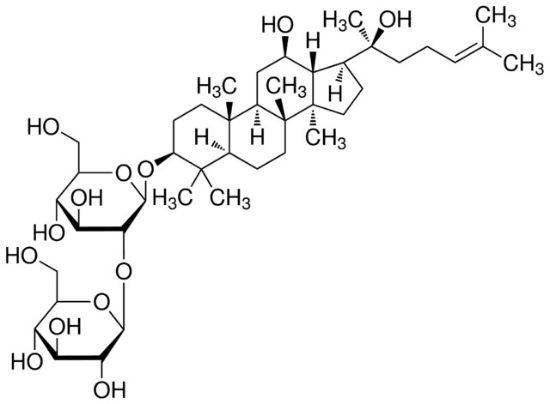
1. 4 фармакокинетика женьшеня Re
Liu et al. [15] studied the pharmacokinetics of ginsenoside Re: новые функцииin humans. After oral administration at a dose of 200 mg·kg-1, the tmax and t1/2 of ginsenoside Re were (1.19 ± 0.44) and (1.82 ± 0.75) h, AUC0-t and AUC0-∞ were (2. 476 ± 2. 281) and (2. 699 ± 2. 284) μg · h · L-1, respectively, ρmax was (0. 939 ± 0. 549) μg · L-1, CL/F was (124 054 ± 84 725) L·h-1. The metabolites of ginsenoside Re in urine were further studied, and three metabolic pathways of ginsenoside Re were inferred: ① Re→Rg1→F1→PPT, ② Re→Rg2→Rh1→PPT, and ③ Re→Rg1→Rh1→PPT. In addition, Joo et al. [16] found that ginsenoside extract can promote the absorption of ginsenoside Re. Ginsenoside Re was administered orally at doses of 10 mg·kg-1 and 50 mg·kg-1, the absolute bioavailability of ginsenoside Re in ginseng saponin extract in rats (0.33% and 0.75%) was higher than that of its monomer administered orally (0.28% and 0.19%).
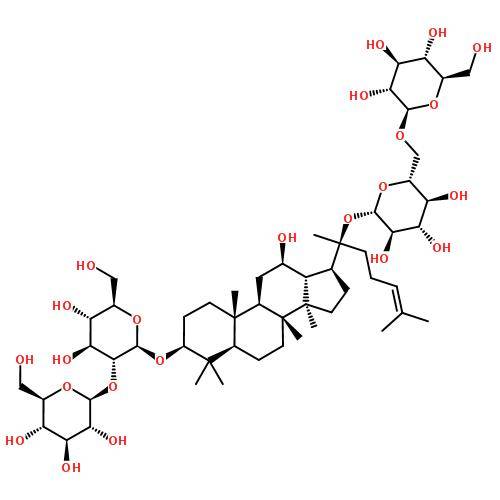
1.5 фармакокинетика женьшеня Rb1
Женьшень Rb1 является основным протоанаксадиол сапонин. Qian et al. [17] изучали метаболиты женьшеносида Rb1 в крысиной крови, фекалиях и моче. Внутривенное введение (5 мг · кг -1) женьшенозида Rb1 в основном метаболизируется в организме крыс путем окисления; В то время как после перорального введения (100 мг · кг -1) женьшеня Rb1 в крысиных фекалиях были обнаружены метаболиты Rd, Rg3, F2, Rh2 и C-K. Предполагается, что метаболический путь Rb1 в кишечнике крыс: Rb1 → Rd → Rg3 или F2 → Rh2 или C-K → PPD. Метаболиты в моче крыс аналогичны метаболитам в фекалиях. Разница между метаболитами перорального и внутривенного введения состоит в Том, что женьшень Rb1 метаболизируется главным образом путем удаления сахарной группы в желудочно-кишечном тракте.
1. 6 фармакокинетика Rh2 женьшеня
Gu et al. [18] исследовали распределение Rh2 женьшеня у крыс. После единичного перорального введения женьшеня Rh2 (3 мг · кг -1), наибольшая концентрация была обнаружена в печени, в то время как концентрации в сердце, селезенке, желудке и почках были аналогичны концентрации в крови. Небольшое количество было распределено в яичниках, надпочечниках и жирах, в то время как Rh2 не был обнаружен в мозге, коже, мышцах и яичниках.
1. 7 фармакокинетика женьшеносида Rd
Женьшень Rd (10 мг · кг -1) вводился внутривенно в организм человека, и пиковое значение было достигнуто через 0,5 ч, с ρmax (2 841,18 ± 473,03) нг ·mL-1 и t1 /2 is (19). 29. (подпись) 3. 44 h, аук0 - т is (27) 161. 63. 8. 116. 88. Управление верховного комиссара организации объединенных наций по делам беженцев ng · h · ML-1, а также дальнейшие исследования показали, что независимо от того, применяется ли женьшень сапонин Rd перорально или внутривенно, метаболиты, такие как Rg3, Rh2, Rd и Rb1, могут быть обнаружены в моче крыс [19]. Ван и др. [20] исследовали фармакокинетику женьшеня Rd у собак с использованием внутривенного (0,2 мг · кг -1) и перорального (2 мг · кг -1) введения. Аук женьшень Rd после внутривенного и перорального введения у собак был (76,451.1 ± 15,874,8) и (1,930,3 ± 647,4) нг · ч ·mL-1, соответственно, и абсолютная пероральная биодоступность составила 0,26%.
2 фармакокинетические исследования женьшеня в традиционной китайской медицине соединение
Комплекс традиционной китайской медицины является основой теории традиционной китайской медицины, а также центром и очагом исследований в области современной традиционной китайской медицины. В последние годы исследователи также изучали фармакокинетику женьшеня в составе. Цзян цзе и др. [21] изучал фармакокинетические характеристики шэнмай инь (препарат традиционной китайской медицины, состоящий из женьшеня, опиопогон японикуса и шисандра чиненсис, с женьшень в качестве основного ингредиента) у человека. После одноразовой пероральной дозы в 300 мл шэнгмай инь была введена 12 здоровым добровольцам, фармакокинетические профили женьшень Rg1 и Re оба следуют однокупе модели.
Средние пиковые периоды tmax для Rg1 и Re составляли (4). 86. 1. 07. И (4). 75. 1. 04. H, соответственно, и средние пиковые концентрации ρmax были (26). 33. 12. 74. И (43). 32. 16. 47. · м -1, соответственно. Период полураспада t1/2ke был равен 7. 99. - 4. 63. И (7). 91. 4. 56. H, соответственно, CL для очистки была (2). 73. 2. 50. И (1). 23. 1. 12 мл · н -1, соответственно, и видимый объем дистрибутива V был (31). 10. 32. 26. И (11). 96. 9. 40 мл, соответственно. С 0 по 30 были (205). 96. 114. 57. И (338). 73. 89. 10. μg · h · mL-1, соответственно.Женьшень saponins Rg1 и ReПодлежат первоклассному кинетическому всасыванию и удалению в организме человека. Между тем, лин ли и др. [22] использовали модель sac кишечника крыс для изучения воздействия соединения женьшень на абсорбцию женьшеня женьшеня Rg1, Re, Rb1 и Rd. Результаты показали, что по сравнению с одним компонентом, соединение группа малых доз (0). 281 мг · мл -1 может способствовать всасыванию женьшеня Rg1, Re, Rb1 и Rd, входящих в группу средних доз соединения (0). 563 мг · мл -1 и группа высоких доз (1). 125 мг · мл -1 не показали значительных различий в абсорбции четырех ингредиентов, и поглощение этих четырех ингредиентов, как правило, сдерживается с увеличением совокупной дозы.

3 факторы, влияющие на фармакокинетику женьшеня
Всасывание и распределение лекарственных средств является очень сложным процессом, и его влияние включает различия между видами в субъектах, формах дозировки лекарственных средств, путях введения и дозах.
3. 1 1 2 3
Due to species differences among the test animals, the pharmacokinetic models of ginsenosides in different test animals are different. Gu et al. [18] studied the pharmacokinetic of ginsenoside Rh2 in dogs and rats. The pharmacokinetic model of ginsenoside Rh2 after intravenous injection in Beagle dogs (0.1 mg·kg-1) was a three-compartment open model, while in rats (0.1 mg·kg-1) it was a two-compartment model.
3. 2 дозировка препарата
Форма дозировки оказывает значительное влияние на фармакокинетику испытуемого препарата. Изменения в дозировке препарата приведут к изменениям фармакокинетических параметров. Препараты женьшеня сапонина не являются исключением. Rode Feng et al. [23] исследовали скорость высвобождения in vitro и абсорбционные характеристики твердых липидных наночастиц женьшеня Rd (Rd-SLN) в различных сегментах кишечника крыс и сравнивали их с мономерами женьшеня Rd. Суммарный уровень высвобождения препарата Rd-SLN после 120 ч составил (89,6/1,6%) %, в то время как раствор для контроля за дезодорантами беременности и родами был почти полностью выпущен (97,21/1,19%) в той же среде после 12 ч. Коэффициенты всасывания Rd-SLN и Rd в кишечных отрезках крыс также были различными.
Между двумя сегментами двенадцатиперстного и желтого не было существенных различий в абсорбции, и разница в показателях поглощения этих двух сегментов была значительной в сегментах илеума и толстой кишки. При тех же условиях дозировки пиковая концентрация крови группы Rd-SLN была значительно выше, чем у группы Rd, а t1/2 и MRT были значительно продлены. В первом случае аумк, аук0 - т и аук0 были примерно в 2 раза, в 1,5 раза и в 2 раза больше, чем во втором. Результаты показывают, что Rd-SLN может замедлить выпуск препарата, увеличить всасывание препарата в кишечник, значительно улучшить биодоступность перорального введения и продлить его период полураспада в крови. Кроме того, гу и др. [18] исследовали изменения в фармакокинетических параметрах 20(R)- Rh2 женьшеня до и после микронизации бигл-собак. Собакам бигл вводили перорально (1 мг · кг -1) 20(R)- гоз женьшеня и его микронизированный порошок, соответственно, отбирали и тестировали на 0,25, 0,5, 0,75, 1,0, 1,5, 2, 3, 5, 7, 9, 12, 24 и 36 ч после введения препарата. Результаты показали, что ρmax, AUC и биодоступность микроэлементов 20(R)- женьшень Rh2 были примерно в два раза больше, чем первоначальный препарат, что указывает на то, что микроэлементы 20(R)- женьшень Rh2 может растворится лучше в кишечной жидкости и войти в кровь легче.
3. 3 административных маршрута
Гу и др. [24] исследовали фармакокинетические изменения женьшеня 20(R) -Rh2 после перорального и внутривенного введения в собаках Beagle. Фармакокинетическая кривая женьшеня 20(R) -Rh2 после внутривенного введения (0). 1 мг · кг -1 соответствует трехкамерной модели, основные фармакокинетические параметры т1/2, CL и AUC0-∞ были (8). 0 на 2. 8. H, (0.1 ± 0.03) L · kg-1 · h-1, (857.0 ± 209.6) ng · h · mL-1, и длительный период полураспада при окончательной ликвидации, предполагающий, что 20(R) -Rh2 могут в определенной степени накапливаться в организме; А фармакокинетическая модель после перорального введения (1 мг · кг -1) представляет собой двухкамерную модель. Основные фармакокинетические параметры tmax, ρmax, t1/2, и AUC0-∞ are (2.6 ± 1.3) h, (371.0 ± 199.6) ng·mL-1, (5.8 ± 2.6) h, (1215.7 ± 598.6) ng·h·mL−1. Медленное поглощение 20(R)-Rh2 собаками Beagle может быть связано с их низкой растворимостью и дисперсией. Кроме того, из-за флюкса p-гликобелка и метаболического действия кишечной флоры, абсолютная биодоступность препарата у собак-биглей низкая, только (16,1 грав11,3 %). Поэтому при разработке форм дозировки для 20(R) -Rh2 следует принимать во внимание административный метод сокращения преобразования и увеличения поглощения препарата.
3. 4 3. Дозировка
Текущие исследования показали, что для женьшеня одной и той же конфигурации в пределах установленного диапазона доз фармакокинетические параметры каждой группы доз увеличиваются с увеличением концентрации дозы, однако существенных различий нет (P > 0). 05. - да. Дэн юаньхуэй и др. [25] изучали фармакокинетические характеристики инъецирования женьшеня после одноразового внутривенного вливания 12 здоровых китайских добровольцев. Результаты показали, что основные фармакокинетические параметры трех доз (10, 40, 75 мг · кг -1): градиент Макс (2,84 градиент 0,47), (10,48 градиент 1,74), (19,34 градиент 2,62) мг · л -1, и т1/2 были (19,29 градиент 3,44), (18,41 градиент 2,92), (17,67 градиент 2,01) н, и аук0 - т были (27,26 градиент 8,12), (112,62 градиент 24,08) и (208,36 градиент 51,36) мг · ч · л -1, соответственно. ρmax, AUC0-t и доза имеют хорошую линейную зависимость, увеличивая пропорционально с увеличением дозы препарата. После коррекции дозы и естественного преобразования логарифма нет существенной разницы между тремя дозами каждого параметра путем анализа дисперсии. Пэн ин и др. [26] изучали фармакокинетические характеристики женьшеня Re в различных дозах у крыс. После внутривенного введения трех различных доз (20, 30, 40 мг · кг -1) женьшеня Re фармакокинетика трех групп крыс была двухкамерной. T1/2 α было 6.505, 6.817, и 4.499 мин, t1/2 β было 28. 96, 30 лет. 49 и 27. 57 мин, соответственно, и аук 599. 31, 1 025. 65 и 1 415. 7 мин · мг · л -1, соответственно. Основные кинетические параметры трех групп крыс были схожими, и аук увеличивался пропорционально увеличению дозы, что указывает на линейную ликвидацию Re в этом диапазоне доз.
4 новые идеи для фармакокинетического исследования женьшеня
4.1 фармакокинетическое исследование метаболитов
В настоящее время пероральное введение является основным методом применения большинства соединений сапонина. Исследования показали, что после перорального введения сапониновые соединения легко метаболизируются кишечной флорой, а концентрация в крови исходного препарата низкая. Поэтому некоторые ученые изучили фармакокинетику женьшеня путем измерения концентрации крови их метаболитов. Рен и др. [27] разработали метод HPLC-APCI-MS для определения 20(S)- протопанаксиола (PPD) в плазме и изучили фармакокинетические характеристики PPD после перорального введения крысам. Результаты показали, что состояние PPD у крыс было (130,2 (41,5) нг ·mL-1 и tmax был (150,0 (73,5) мин. Абсолютная биодоступность PPD была (36,8 (12,4)%, в 10 раз больше, чем у его prodrugs женьшень Rg3 и Rh2, что указывает на то, что PPD легче всасывается в кровоток. Поэтому измерение концентрации крови PPD может более точно отражать фармакокинетические характеристики женьшеня Rg3 и Rh2.
4.2 фармакокинетика различных моделей заболеваний
В модели синдрома фармакокинетический процесс традиционной китайской медицины отличается от обычного физиологического процесса животных. Поэтому более поучительно изучать фармакокинетику традиционной китайской медицины на основе синдромов. Чжоу вэй и др. [28] изучали фармакокинетические изменения эффективных компонентов клыка циннао сюаньцяо, включая садовник, женьшень Rg1, Rb1 и нотоженьшень R1, у крыс в нормальных условиях и на острых и восстановительных стадиях инсульта. Результаты показали, что эффективные компоненты формулы Qingnao Xuanqiao: gardenia, женьшень saponin Rg1 и notoginseng saponin R1 являются двухкамерными открытыми моделями в обычной группе и группе моделей, а женьшень saponin Rb1 соответствует однокамерной модели. Поглощение четырех компонентов крыс было быстрым, достигнув ρmax примерно за 45 минут. Удаление садовой части, женьшень Rg1 и нотоженьшень R1 происходит быстрее, в то время как женьшень Rb1 происходит медленнее. Для различных животных модели максимальная концентрация крови и область под кривой "концентрация-время" крови четырех компонентов, от самой высокой до самой низкой, являются острой группой моделей > Модель восстановления > - обычная группа. Биодоступность модельной группы к препарату выше, чем у обычной группы, что указывает на то, что у модельных животных наблюдается повышенная абсорбция клыка циннао сюаньцяо по сравнению с обычными животными.
4. 3 многокомпонентная комплексная фармакокинетика
Влияние традиционной китайской медицины имеет механизм многокомпонентных и многоцелевых эффектов. Более односторонним является объяснение фармакокинетического процесса традиционной китайской медицины и рецептов по фармакокинетическим параметрам одного компонента. Поэтому ли сяоюйю и др. [29] использовали panax notoginseng saponins в качестве типового препарата для создания комплексной фармакокинетической исследовательской модели на основе площади под кривой (AUC0-∞) каждого компонента panax notoginseng saponins с custom весового коэффициента. Крысам вводили Panax notoginseng total saponins (300 мг · л -1) через гаваж и (10 мг · л -1) внутривенно, а концентрации notoginsenoside R1, женьшень Rg1, Rd, Re и Rb1 в крысиной плазме определялись с использованием LC-ESI-MS. После введения через гаваж общее количество сапонинов нотожензенга быстро всасывается в организм крыс, но t1/2 диола сапонинов Rb1 и Rd значительно больше, чем у триола сапонинов Rg1, Re и R1, Результаты комплексной фармакокинетической исследовательской модели, разработанной с использованием процентной площади под кривой (AUC0-∞) каждого компонента в качестве самостоятельного весового коэффициента, показали, что комбинированная кривая "концентрация-время" соответствует закону о ликвидации лекарственных средств, применяемых путем гаважа или внутривенной инъекции. Panax notoginseng общее количество сапонинов быстро всасывается крысами. Комплексные фармакокинетические т1/2 и аук после гаважа и внутривенного введения составили 18,88 и 19. 15 ч. 25 м. 33, 84 года. 83 мг · ч · л -1, соответственно. Эта модель соответствует характеристикам классических фармакокинетических моделей, и полученные параметры в наибольшей степени характеризуют общее состояние традиционной китайской медицины. Это дает новую исследовательскую идею и метод для организации фармакокинетических исследований в области традиционной китайской медицины, которые соответствуют характеристикам традиционной китайской медицины.
5. Перспективы на будущее
Женьшень имеет разнообразную биологическую деятельность и значительную клиническую эффективность. Были проведены обширные исследования их фармакологических эффектов и фармакокинетического поведения, и были достигнуты некоторые результаты. Однако некоторые области все еще нуждаются в улучшении.
On the one hand, ginsenosides are easily metabolized by the gastrointestinal tract and liver, and their blood concentrations in the body are low and not easy to detect. Therefore, modern high-sensitivity analytical techniques (GC-MS/MS, LC-MSn, LC-NMR, etc.) need to be applied to the detection of ginsenosides in vivo. At the same time, since the substances that exert effects on target tissues in vivo may be their metabolites, attention should also be paid to the detection and analysis of ginsenoside metabolites. On the other hand, pharmacokinetic studies of ginsenosides at home and abroad have only studied the relationship between blood concentration and time from a chemical perspective [15, 21], ignoring the connection with efficacy.
Поэтому в будущих исследованиях фармакокинетику женьшеня следует сочетать с фармакодинамическими показателями для изучения трехмерной взаимосвязи между концентрацией-временным эффектом и создания одновременно фармакокинетической и фармакодинамической модели анализа, тем самым более реалистично и объективно отражая фармакокинетический процесс женьшеня в организме и обеспечивая определенную основу для клинической эффективности. Кроме того, существует множество типов женьшеня в традиционной китайской медицине женьшеня, и фармакокинетические параметры каждого индивида различны [30], которые не могут быть использованы для характеристики общего фармакокинетического поведения и характеристик женьшеня. Поэтому мы должны руководствоваться теорией традиционной китайской медицины и сочетать современные экспериментальные методы, такие как метаболика, протеомика и генные чипы, для изучения новых методов фармакокинетических исследований многокомпонентных компонентов традиционной китайской медицины с системной биологической точки зрения [31].
Ссылка:
[1] Чжан г, лю а, чжоу и др. panax женьшень женьшень-Rg2 Защищает от повреждения памяти с помощью антиапоптоза в крысиной модели С сосудистым слабоумием [J]. - J.этнофармакол,2008,115 (3) : 441-448.
[2] Ю х т, ван с п. Клиническое наблюдение за лечением постопа-ракового заболевания желудка женьшеносидом Rg3 Объединенные арабские эмираты with Химиотерапия [J]. Предыдущий курс лечения, 2010,17 (10) :779-781.
[3] Чжан (Китай) Z, цзян, Китай - би, чжэн X,et, Al. Иммунитет Повышение эффективности управления Воздействие Rg3 На периферических лимфоцитах in vitro у больных раком Лечение радиотерапией [J]. Чин фарм J, 2004,39(4) : 261-264.
[4] SUI D Y,YU X X X XF,QU S C,et al.Effects of Panax quinquefoli- um 20 -2protopanaxdiol saponins on experimental желудочковый re- моделирование в крысах [J]. Чин фарм J,2007,42 (2) : 108-112.
[5] Li Y,JIN Y,LIM W,et al.A женьшень-rh1, компонент женьшеня Сапонин, активируется - эстроген 3. Рецептор in human Рак молочной железы MCF-7 клетки [J]. J стероидная биохим,2003,84 (4) : 463 — 468.
[6] WILLIAM C S,CHUNG W S,SALLуK W,et al.женьшень Re женьшень Panax обладает значительным антиоксидантом и антихей-перлипидемией Iii. Эффективность in Стрептозотоцин вызывает - диабетик. rats [J]. Eur J Pharmacol,2006,550(1-3) : 173-179.
[7] KIM S E,LEE Y H,PARK H J,et al.ginsenoside rs4,a new Тип женьшеня сапонина одновременно вызывает апоптоз, а selec- значительно повышает уровни белка p53 и p21WAF1 в клетках человека hepato- ma SK-HEP-1 European [J]. Рак,1999,35 (3) : 507-511.
[8] LI H,SUN J G,XIE H T,et al.Study о абсорбционном механизме женьшеня Rg1 Использование программного обеспечения - крысы. В любом случае Гут sac [J]. Чин дж. Клин фармакольный эфир,2004,9 (5) : 510-513.
[9] Фэн л, ху чж, ю л и др. фармакокинетика гинзена-oside Rg1 И метаболитов у крыс [J]. Acta Pharm Sin,2010,45 (5) : 636 — 640.
[10] Ли дж., ли е., ким д., и др. исследования абсорбции, дирибу и метаболизма женьшеня у человека после перорального введения [J]. J этнофармакол,2009,122(1) : 143 — 148.
[11] Париж (Франция) X W,GUI F J,TIAN J M, и др. фармакокинетика женьшеня rg2 У крыс [J]. Чин фармакол булл,2009,25 (7) : 967-970.
[12] GUI F J,YANG X W,LI L Y,et al.одновременное определение энантиомера 20 (р)-и 20 Женьшень-rg2 в крысиной плазме после внутривенного введения с использованием метода HPLC [J]. J хроматография B,2007,850(1-2) : 1-6.
[13] Хуанг (HUANG) Y, лю, J - эйч. Фармакокинетический метод лечения Исследования по теме: Женьшень 20 (S) -Rg3 У крыс с помощью HPLC-ELSD[J]. J Pr Med Theory,2005,12(9) : 2564-2566.
[14] Цай-з, цянь-т, вонг-р и др. жидкая хроматография -elec- тросраспылительная масс-спектрометрия для метаболизма и фарма-кокинетические исследования женьшеня Rg3[J]. Анал ким акта,2003, 492(1-2) : 283-293.
[15] Лю л, хуан дж, ху х и др. одновременное определение женьшеня (G-Re,G-Rg1,G-Rg2,G-F1,G-Rh1) Прото-панакриол в плазме и моче человека лк-мс/мс и его ap- пликация в фармакокинетическом исследовании G-Re у добровольцев [J]. J хроматография B,2011,22(15) : 2011 — 2017.
[16] чжу к, ли чж, чон х и др. фармакокинетическое исследование женьшеня Re with В чистом виде ginsenoside Re and ginseng - ягоды (*) Выдержки из статьи С помощью мыши Использование программного обеспечения - в чем дело? Жидкостная хроматография / Масс-спектрометрический метод [J]. J фармацевтика биомед,2010,51 (1-2) : 278-283.
[17] Цянь т, цзян з х, цай з. Высокопроизводительная жидкая хромография в сочетании с тандемной масс-спектрометрией применяется для мета-болического исследования женьшеносида Rb1 на крысах [J]. Анал биохем,2006, 352(1) : 87 — 96.
[18] Гу й, ван г джей, сун дж. Фармакокинетическая характеристика Rh2 женьшеня, антиканцерогенного питательных веществ из женьшеня, у крыс и собак [J]. Food Chem Toxicol,2009,47 (9) : 2257-2268.
[19] Ян л, Дэн у, сюй с, и др. в vivo фармакокинетические и Исследования метаболизма женьшень Rd [J]. J хроматография B, 2007,854(1-2) :77-84.
[20] 13. ВанW,WANG G J,XIE H T,et al.Determination of gin- senoside Rd in - собака?Плазма и плазмаby liquid chromatography-mass spec- trometry after Твердофазная фаза (твердофазная фаза) 1. Извлечение and its 3. Применение in dog Фармакокинетические исследования [J]. J хроматография B,2007,852 (1-2) : 8-14.
[21] JIANG J,LI S,GONG P L, и al.Pharmacokinetics шэнмайин орального раствора после одной дозы в человека [J]. Акта-мед Сi-Univ < < текнол > > Huazhong, 2007,36(2) : 272-274.
[22] LIN L,ZU F Y,ZHANG W,et al.Effects of compatibility on абсорбция in vitro сапонинов женьшеня [J]. 13 ч. 00 м. - чин J Мод препарат Appl,2010,4 (13) : 150- 152.
[23] LUO D F,YE J T,ZHANGY S, и др. исследования по выпуску наркотиков в vitro and absorption in - крысы. in vivo of ginsenoside Rd твердое вещество - липид. Наночастицы [J]. Чин фармакол булл, 2009,25 (7) : 923-926.
[24] Гу и, ван G J,SUN J G, и др. фармакокинетическое исследование женьшеня 20(R) -Rh2 В Beagle dogs by LC-ESI-MS [J]. Чин дж. Клин фармакольный эфир,2006,11 (3) : 159-163.
[25] - Дэн, Дэн. Y H,ZENG X,FENG Y, и др. фармакокинетика и Допуск на однодозированный внутривенный капель женьшеносида injec- tion в китайских здоровых добровольцах [J]. Чин дж. Клин фармакол,2009,25 (2) : 116-120.
[26] PENG Y,WANG S J,PAN W S, и al.Pharmacokinetics женьшеня Re в крысах [J]. J Shenyang Pharm Univ,2006,23 (4) : 197-200.
[27] REN H C,SUN J G,WANG G J, и др. чувствительность определения Из 20 (S)-протопанаксадиол in rat plasma Использование программного обеспечения HPLC-APCI-MS: Применение фармакокинетического исследования на крысах [J]. J фарм би-гомед,2008,48 (5) : 1476-1480.
[28] Чжоу W, ши R B,SUN J N, и al.Pharmacokinetics effec- тивные фракции Qingnaoxuanqiao формулы в различных моделях крыс [J]. J Beijing Unit Tradit Chin Med, 2008,31 (4) : 265-268.
[29] LI X Y,HAO H P,WANG G J,et al.Integrated pharmacokinet- ic исследование нескольких эффективных компонентов, содержащихся в total panax Notoginsenosides [J]. Чин дж нат мед,2008, 6(5) : 377-381.
[30] Сон м, чжан с, сюй х и др. одновременное определение Из трех сапонинов Panax notoginseng при субнанограммах лк-мс / MS в плазме собаки для фармакокинетики соединения Danshen tab- let [J]. J хроматография B,2010,878 (32) : 3331 — 3337.
[31] WANG Я, ма, X, хэн X,et, Al. Текущий ток В. методы работы and Ad-vancesin microbial metabolom ics[J]. Prog Chen, 2010,22(1) : 163 — 172.


 Английский язык
Английский язык Французский язык
Французский язык На испанском языке
На испанском языке Русский язык
Русский язык Корейская народно-демократическая республика
Корейская народно-демократическая республика На японском языке
На японском языке




