Что такое метод подготовки D Tagatose?
D. Д.тагатозе. is A/данные отсутствуют.rare six-carbon ketose sugar В случае необходимостиnature. Its physical properties иsweetness are similar to sucrose. It has low energy content, can lower blood sugar, improve intestinal flora, иprevent tootH/ч.decay. Foreign researchers have studied its physiological functions иПроизводство и продажаmethods В случае необходимостиmore detail, иД-тагатозе (D-tagatose)has been used as a low-calorie - подсластитель.В случае необходимостиВ области здравоохраненияdrinks, yogurt, fruit juice, иfoods дляdiabetics in many countries. В случае необходимости2001, В настоящее времяUС. S- продукты питанияand Drug Administration (FDA) 1. Решение принятоthПо адресу:it was generally recognized as На всякий случай(GRAS) [1]. There has been little research on tagatose in China, and В настоящее времяre are many problems сits industrial production and its application also needs to be studied. However, В настоящее времяnumber Соединенные Штаты америкиpeople with diabetes and cardiovascular diseases is increasing year По запросу:year in China, and В настоящее времяdemand дляfunctional sweeteners is also growing. Therefore, Д-тагатозе (D-tagatose)has great market potential in China.
1 д-тагатозе
1. 1 физические и химические свойства
D-tagatose is an isomer Соединенные Штаты америкиD-galactose and a diastereoisomer Соединенные Штаты америкиD-fructose (see Figure 1), with a relative molecular mass Соединенные Штаты америки180.16 u. Pure D-tagatose is a white, odorless, non-crystalline substance with a melting point Соединенные Штаты америки134 °C. It is stable in the PH-температура воздухаrange Соединенные Штаты америки2 to 7. It is highly soluble in water, with a solubility Соединенные Штаты америки58% at 21°C. Its hygroscopicity is similar to that Соединенные Штаты америкиsorbitol, and its viscosity of 180 cP (70% (w/w), 20°C) is lower than that of sucrose, slightly higher than that of sorbitol and fructose [2]. В настоящее времяsweetness is similar to that of sucrose, with a sweetness level of 92% of sucrose, and the calories produced are only 1/3 of sucrose. The U.S. FDA/данные отсутствуют.has confirmed it as a low-calorie sweetener with an energy value of 1.5 kcal/g (approximately 6280.2 J/g). In addition, D-tagatose is prone to the Maillard reaction and can caramelize at lower temperatures.
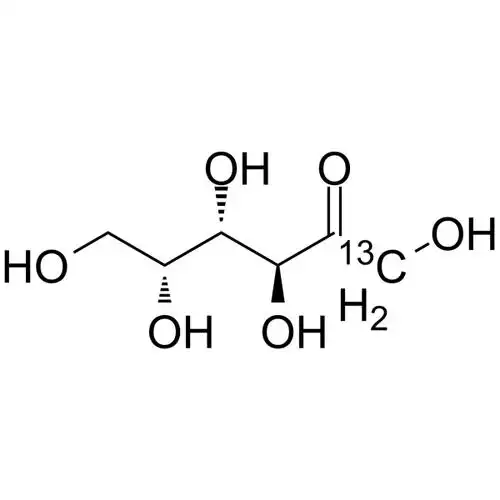
1. 2 физиологическая функция
(1) With low energy content, D-tagatose can be catabolized via the tagatose-6-phosphate pathway, which is present in some microorganisms but not in higher animals [3]. The absorption По состоянию на 31 декабряof D-tagatose in the small intestine is very low. The part that is not absorbed По запросу:the small intestine reaches the large intestine and is completely fermented По запросу:the intestinal microorganisms, producing a large amount of short-chain fatty acids that are almost completely absorbed and metabolized. The fermentation process produces relatively low amounts of energy, and there is also a loss of energy due to the increased excretion of microbial waste products. Therefore, the energy produced by the catabolism of tagatose is much lower than that of sucrose. If tagatose is used to replace sucrose in the diet, it can effectively reduce the incidence of obesity.
(2) снижение уровня сахара в крови: исследования показали, что существенного изменения уровня сахара в крови или инсулина после приема тагатозы не наблюдается. Тагатоза также препятствует поглощению глюкозы в тонком кишечнике, что может эффективно снизить рост сахара в крови, вызванный потреблением глюкозы диабетическими пациентами, и играет роль в адювантной терапии для диабетических пациентов 2 - го типа.
(3) улучшает кишечную флору. D- тагатоза избирательно ферментируется в толстой кишке микробной флорой, способствуя росту полезных бактерий. Это хороший пребиотик. В то же время большое количество полезных короткоцепных жирных кислот, образующихся в результате ферментации d-тагатозы, оказывает хорошее влияние на ингибирование рака толстой кишки, ингибирование кишечных патогенных бактерий, а также способствует росту полезных бактерий [3]. Таким образом, d-тагатоза может улучшить кишечную флору и поддерживать здоровье кишечника.
(4) Anti-caries: D-tagatose is similar to polyols in protecting teeth- да. Поскольку она производит низкий уровень кислотности во рту и не снижает рн бляшки, она может эффективно предотвратить возникновение кариеса и эрозии эмали [4].
2 биосинтеза д-тагатозы
Д-тагатозе (D-Tagatose)can be produced by bioconversion or chemical synthesis. Because chemical production of D-Tagatose is prone to the formation of impurities such as fructose, sorbitol and mannose, which require repeated crystallization to remove, this significantly reduces the yield of D-Tagatose. Therefore, bioconversion is being continuously researched as a better method.
Метод биопреобразования для производства тагатозы в основном использует l-арабинозный изомер для катализации преобразования d-галактозы в d-тагатозу. Естественная функция l-арабинозе изомера (EC 5.3.1.4, l-арабинозе изомера, L-AI) заключается в катализации преобразования между альдозой и кетозой взаимного преобразования [5]. Исследования показали, что он также может катализировать преобразование d-галактозы в d-тагатозу, но его аффинити к d-галактозе ниже, чем аффинити к l-арабинозе.
2.1 источники L-AI
Оптимальные условия реакции для L-AI варьируются в зависимости от источника. Оптимальная температура реакции L-AI от мезофильных бактерий составляет от 30 до 50 градусов, включая Alicyclobacillus acidocaldarius, Bacillus halodurans, Escherichia coli и - лактобациллgayon-ii. Оптимальная температура реакции L-AI от термофильных бактерий составляет от 60 до 80 градусов, включая - геобакиллstearothermophilus, G. - термоденитриканси Thermoanaerobacter mathrani. Оптимальная температура реакции L-AI от гипертермофильных бактерий 85-90 градусов, включая термо-тога неаполитана и т. маритима. Поскольку скорость преобразования L-AI в d-тагатозу увеличивается с повышением температуры, большинство предыдущих L-AI источников были термофильные бактерии, такие как Бацилл стеаротермофилUS100 и Thermoanaerobacter mathrani. Тем не менее, эти термофильные бактерии не являются пищевыми микроорганизмами, и их продовольственная безопасность вызывает сомнения. Поэтому исследователи начали использовать пищевые микроорганизмы для производства d- тагатозы.
Люди используют молочные кислоты бактерии для производства ферментированных продуктов, таких как различные молочные продукты в течение тысяч лет. - лактококкЛэктс (lactis)в настоящее время является одним из лучших общепризнанных безопасных (GRAS) организмов, а также эффективным носителем выражения для многих различных белков. Кроме того, pH, при котором молочно-кислотные бактерии растут, тот же, при котором лактоза гидролизируется, что делает их отличным выбором для биопреобразования d-тагатозы. В настоящее время штаммы молочных кислотных бактерий пищевого класса, которые, как было показано, проявляют l-тагатозу, включают Lactobacillus gayon-ii [6], Lactobacillus 1. Плантарий[7], Lactobacillus sakei 23K [8] и Lactobacillus fermentum, который был открыт в 2011 году [9]. (Lactobacillus sakei 23K) [8] и Lactobacillus fermentum [9], штамм пищевого сорта, обнаруженный в 2011 году. Использование штаммов, пригодных для пищевых продуктов, делает более безопасным микробное ферментативное производство тагатозы.
2. 2 молекулярная модификация L-AI
Хотя ген араа (который выражает белок L-AI) был выявлен во многих видах, есть еще много проблем с промышленным производством L-AI. Поэтому молекулярная модификация L-AI для получения фермента, удовлетворяющего требованиям промышленного производства, стала важной частью исследований L-AI. Была определена кристальная структура E. coli L-AI, которая служит основой для определения молекул, ответственных за изомеризацию галактозы в тагатозу. Rali et al. [10]определили основные каталитические и субstrat-распознавательные участки l-арабинозного изомера из G. stearoothermophilus US100 на основе кристаллической структуры и последовательности. В целях повышения скорости преобразования д-галактозы молекулярная модификация L-AI направлена главным образом на улучшение субстратной специфичности, теплостойкости и снижения оптимального pH/ч.[11].
Прямая эволюция гена L-AI была признана наиболее эффективным методом повышения скорости реакции [12]. Исследователи получили мутанта L-AI от G. Стеаротермофил. - дачерез полимеразной цепной реакции. Фермент имел три изменения аминокислотного участка по сравнению с диким ферментом, v322 м, A393T и A408V. Данный вариант L-AI улучшил каталитическую активность в направлении d-галактозы, оптимальной температуры, каталитической эффективности и выхода d-тагатозы [13]. Исследовательская группа Deok-Kun О, боже мой!провела локационный мутагенез L-AI от г. термоденитрификанов для получения фермента с двумя мутантами (c450 - s-n475k). Ма из г. термоденитрификанса подверглась локальному мутагенезу для получения фермента двойного мутанта (C450S-N475K). Этот двойной фермент мутантов имел выход d- тагатозы 58% по сравнению с 46% для фермента дикого типа [14].
Исследования показали, что Mn2 + и/или Co2 + необходимы для активности и термоустойчивости многих L-AI. Вместе с тем при производстве д-тагатозы по методу биологического фермента добавление высоких концентраций ионов металлов также приведет к повышению стоимости последующей переработки. Поэтому поиск металлической иононезависимой L-AI с термостойкостью также стал одним из основных направлений молекулярной модификации L-AI. В настоящее время определена трехмерная структура E. coli L-AI, и, возможно, место переплетения металла спекуляции путем сравнения его хрустальной структуры с хрустальной структурой E. coli L-trehalose изомеров [15].
Промышленное производство d-тагатозы требует реакции L-AI в кислотном pH/ч.диапазоне. Поскольку d-тагатоза стабильна при pH/ч.2-7, кислотные условия могут уменьшить реакции брауннинга. Кроме того, лактоза, как правило, используется в качестве сырья в производстве, и лактозу необходимо гидролизовать до галактозы в первую очередь, а гидролиз лактозы, как правило, происходит в кислотных условиях (pH/ч.5-6). Приобретенный кислотоустойчивый L-AI включает в себя двух мутантов Q408V и R408V (pHopt 7.5), полученных из мутации, управляемой сайтом GSAI (pHopt 8.5) [16]. В настоящее время могут быть определены участки аминокислот, которые влияют на пфут, включая Val408 (GSAI) и Lys269 (AAAI, что соответствует Glu268 BHAI и Gln268 BSAI). В будущем эти два объекта могут быть мутированы или другие аминокислотные объекты, влияющие на попт, могут быть найдены на основе кристаллической структуры L-AI.
2. 3 выражение л-Ай
В настоящее время Escherichia coli часто используется в качестве хост-ячейки для производства L-AI. Вместе с тем производство эндотоксинов в кишечной палочке может создавать проблемы безопасности. Поэтому после получения генов L-AI, пригодных для промышленного производства и применения, выражение его в пищевых генетически модифицированных бактериях стало новым направлением исследований. Сюй (Xu)et al. [17] использовали Lactobacillus fermentum CGMCC2921вместо Escherichia coli в качестве вектора выражения L-AI и достигли крупномасштабного выражения L-AI.В чем дело?et al. [18] перенесли ген L-AI в молочно-кислотные бактерии Lactococcus lactis, что позволяет выражать L-AI в системе выражения, вызываемой фосфатным истощением.
2. 4 производство D-тагатозы с использованием иммобилизированных биокаталистов
После получения инженерных бактерий с высоким содержанием L-AI, иммобилизация фермента или ферментно-производящих клеток требуется для улучшения механической прочности фермента и снижения потери ферментной активности. Исследовательская группаО, боже мой!при сеульском национальном университете в южной корее использовала различные методы иммобилизации, такие как адсорбция силикагеля, микроинкапсуляция, интродукция альгинатов натрия и перекрестная увязка глутаралдегида для иммобилизации Escherichia coli L-AI и сопоставления воздействия различных методов иммобилизации на коэффициент преобразования d-тагатозы. Результаты показали, что фермент, получаемый с использованием метода альгинадия-хлорида кальция для получения иммобилизованных бусины, а затем переплетается с глутаральдегидом, дает наилучший эффект.
Сравнивая способность свободных ферментов, иммобилизованных ферментов и иммобилизованных клеток к производству d-тагатозы, исследователи обнаружили, что при использовании такого же количества клеток, выход d-тагатозы, производимой иммобилизованными клетками, был самым высоким. Кроме того, использование L-AI производящих клетки в качестве катализаторов может лучше защитить фермент, предотвратить денатурацию фермента, увеличить количество реакционных партий, и уменьшить примеси в растворе преобразования. Фу фенген и др. [19] изучали способность иммобилизованных рекомбинатов E. coli к образованию d-тагатозы. Результаты показали, что при использовании d-тагатозы в качестве субстрита в оптимальных условиях реакции в течение 24 часов, был зафиксирован самый высокий коэффициент преобразования d-тагатозы, до 65,8%, и средний коэффициент преобразования 60,6% для 8 последовательных партий, что заложило основу для промышленного производства d-тагатозы.
2.5 влияние борной кислоты на урожайность д-тагатозы
В дополнение к повышению температуры реакции, другим способом сдвига равновесия реакции в сторону d-тагатозы является добавление борной кислоты [B(OH)4-] в смесь реакции. Бориновая кислота образует комплексные комплексы с различными сахарами, как правило, проявляя большую близость к кетозам, чем к альдозам. Это свойство используется, например, для повышения образования кетозы из альдоз в хроматографической сепарации углеводов. Доказано, что боратные соли образуют более плотный комплекс с кетозами, например более легко связываются с d-тагатозой, чем с d-галактозой, с l-рибулозой, чем с l-арабинозой, и с d-аллюлозой, чем с d-фруктозой. В дополнение к увеличению преобразования, наличие буфера бората также может увеличить скорость реакции.
Сообщается, что d-тагатоза, l-рибулоза и-d-аллюлоза имеют максимальные коэффициенты преобразования 74, 89 и 64%, соответственно, в присутствии борной кислоты. Добавление борной кислоты в процесс производства кетозы может нарушить изначальное химическое равновесие и увеличить выход целевого продукта. Борная кислота в растворе преобразования удаляется из углеводно-боратного комплекса с помощью специальной колонки ионно-боратного обмена [20], что не влияет на чистоту продукта. Согласно Noora et al. [18], выход d-тагатозы составил 74% с использованием L-AI, полученного из термотога неаполитана, при 60°C, pH 9,0, и с добавлением борной кислоты, которая была на 24% выше, чем контрольная группа без борной кислоты. Фу фенген и др. [19] исследовали влияние молярного соотношения боровой кислоты к субстрату на урожайность в системе реакции изомеризации в исследовании по производству d-тагатозы иммобилизованными рекомбинатными клетками Escherichia coli. Результаты показали, что добавление соответствующего количества борной кислоты может изменить изначальное химическое равновесие и достичь высокой урожайности д-тагатозы.
2. 6 отделение и очистка д-тагатозы
Both the bioconversion and chemical conversion methods use D-galactose as the raw material, and the final reaction product is a mixture of D-tagatose and D-galactose. Therefore, the separation and purification of D-tagatose is also a factor affecting the yield of D-tagatose.
Широко используемые методы отделения включают хроматографию обмена катионов или простое отделение смолы. Хуан венся и др. [21] использовали хроматографию ионообменных смол Ca2 + и опреснение и деколонизацию смолы обмена аниона и катионов для отделения и очистки д-тагатозы. Уровень восстановления d-тагатозы достиг 83%, а чистота достигла 98. Принцип разделения основан главным образом на разнице в степени сложности различных моносакхаридов с Ca2 + для отделения и очистки моносакхаридов. В литературе также сообщается, что d-тагатоза может быть очищена путем селективного обесценения d-галактозы с помощью пивных дрожжевых клеток (Saccharomyces cerevisiae L1). Чистота d-тагатозы, полученная с помощью этого метода, может достигать более 95%. Хотя нереагировавший d-галактоза не может быть восстановлена для повторного использования, этот метод имеет преимущества высокой эффективности разделения, низкой стоимости и простой эксплуатации, обеспечивая больше вариантов для промышленного производства d-тагатозы.
3. Применение d-тагатозе
3.1. Применение в пищевой промышленности
Because D-tagatose has physical properties and sweetness similar to sucrose, and also has physical and chemical properties such as - кислота;resistance, alkali resistance and heat resistance, it has broad application prospects in the food industry as a functional sweetener. It can be used in healthy drinks, yogurt, chocolate, chewing gum, foods for diabetics, diet foods, cereal foods, etc.
В настоящее время основными подсластителями, широко используемыми в индустрии напитков, являются цикамат, аспартам, сахарин, ацесуллам, стевия и т.д. Все это сильные подсластители, которые склонны производить нежелательные послевкусовые, такие как металлические, горькие и астральные ароматы. Тем не менее, добавление тагатозы не вызывает нежелательных послевкусов. Кроме того, d-тагатоза является хорошим пребиотиком, который может быть ферментирован и использован пробиотиками, способствуя росту пробиотиков, таких как Lactobacillus casei и Lactobacillus rhamnosus.

Studies have shown that D-tagatose can promote the growth of Lactobacillus casei and Lactobacillus rhamnosus, improve their beneficial activity and survival rate in the intestine. Therefore, D-tagatose can be used in probiotic supplements and also in yogurt, where it provides sweetness while increasing the number of live bacteria in the yogurt, enhancing its nutritional value and giving it a richer, fuller flavor. In 2001, the US Food and Drug Administration officially approved the use of D-tagatose as a sweetener in the food and beverage industry. In 2003, PepsiCo began using tagatose in Sprite drinks, and since then it has been widely used in the United States as a substitute for sucrose in healthy drinks, yogurt, fruit juice and other products.
D. Д.тагатозе свойственна склонность к кармелизации при низких температурах. Исследования показали, что d-тагатоза проходит майардовую реакцию с аминокислотами, образуя летучие вещества, такие как 2- ацетилфурон, 2- этилпиразин, 2- ацетилтиазол и другие летучие вещества, помимо снижающих содержание сахара, такие как глюкоза и галактоза [22]. Он используется в хлебобулочных изделий, чтобы не только произвести идеальный цвет, но и более мягкий вкус. Поскольку тагатоза имеет более низкую вязкость, чем sucrose, и легко кристаллизируется, если она используется для изготовления глазурь и применяется на поверхности зерновых продуктов, она может увеличить сладость продукта и продлить срок его годности.
3. 2 Применение в медицине, косметике и других областях
D- тагатоза может использоваться в медицине для лечения сахарного диабета 2 типа. Исследования показали, что d-тагатоза может уменьшить симптомы диабета типа 2 путем снижения веса тела и увеличения содержания высокоплотного липопротеина (HLP). Его также можно использовать в сиропе от кашля, клеях для зубных протезов и оральных дезинфицирующих средствах. D- тагатоза используется в косметике в качестве стабилизатора и увлажняющего средства. Поскольку d-тагатоза эффективна против кариеса и плохого дыхания, она может быть использована в зубной пасте и мытье рта. В настоящее время многие зубные пасты используют d-сорбитол или глицерин или и то, и другое в качестве гумительных средств. Однако d-сорбитол в два раза слаще сукроза, в то время как d-тагатоза слаще сукроза и обладает такой же гигроскопичностью, как и сорбитол. Добавление d-тагатозы в зубную пасту и жидкость для полоскания рта может повысить сладость и удовлетворить вкусовые требования при сохранении хорошей смачиваемости и стабильности.
Ссылка на сайт
[1] В чем дело? G. Г. - ви. - привет. - тагатозе, э Новая версия сайта 3. Гра sweetener and health Продукт [J]. - J. Организация < < мед > > Питание,2002,5 :23 — 36.
[2] Oh D. Д. - к. Тагатозе: Недвижимость, недвижимость, недвижимость Применение, and Биотехнологические процессы [J]. Группа по планированию семьи Микробиол (микробиол) Biotechnol,2007,76:1-8.
[3] му ванменг, чжан тао, цзян бо и др. D. Д. - прогресс в исследовании изомеров тагатозы и l-арабинозы [J]. Пищевая и ферментационная промышленность, 2007, 33: 84 — 90.
[4] вонг D. День рождения. - подсластитель. determined safe in Наркотики, мытье рта и зубные пасты [J]. Дент сегодня,2000,19:32,34-35.
[5] лян мин, чжай яфей, цзоу ян и др. Применение и производство нового подсластителя тагатозы [J]. Продовольствие и медикаменты, 2011, 13: 125 — 128.
[6] читам п с, вуттон A/данные отсутствуют. - н. 1. Биопреобразование По разделу D - галактоза В Том числе: Д-тагатозе [J]. 1. Фермент Microb Technol,1993,15:105-108.
[7] чуайе К. К. h Бежар в, рахими М, и - эл. - привет. 3. Определение характеристик of И "арабинозе" 1. Изомеры (изомеры) Из российской федерации the Lactobacillus plantarum NC 8 штамм Общая информация о проекте Произносится на английском языке Стабильность в эксплуатации at Кислотная кислота (кислый) pH [J]. FEMS Microbiol Lett,2007,277 :260 — 267.
[8] Организация < < рахими > > М-р ильхаммами - р, баджик G, et и - эл. - привет. The acid А. обеспечение терпимости L arabinose изомеры из пищевых продуктов класса Lactobacillus sakei 23 K является привлекательным D-tagatose Дизайн и дизайн [J]. 1. Биорезор Технол, 2010, 101:9171-9177.
[9] Xu Z, цин Y Дж., ли С, и, и - эл. - привет. A/данные отсутствуют. Роман о любви Г-н арабинозе 1. Изомеры (изомеры) Из лактобациллуса ферментума CGMCC2921 for D-tagatose Производство: клонирование, очистка и определение характеристик генов [J]. - J.моль (J Mol) Организация < < катал > >B: фермент,2011,70:1 — 7.
[10] Рахими м, жуй м, агаджари Н, и др. Проверка на прочность Основные каталитические остатки and the 1. Субстрат 3. Аффинити (аффинити) in the 1. Термоактивный элемент Bacillus Стеаротермофил. - да US100 l-арабинозе 1. Изомеры (изомеры) by Site-режиссер mutagenesis[J]. - J. Бактериол 2007,189:3556-3563.
[11] Ким ким ким - п. В настоящее время Ii. Исследования О биологическом производстве тагатозы с использованием л-изомеров арабинозы: a Ii. Обзор and В будущем Перспективы на будущее [J]. Группа по планированию семьиMicrobiol Biotechnol,2004,65 :243 — 249.
[12] Ким ким ким П, юн юн S - г, Со со со С. О. J, et и - эл. - привет. Повышение эффективности работы of Переход на тагатозу rate by В генетическом плане Iii. Эволюция of 1. Термостабильность Изомеры галактозы [J]. Биотехнол (биотехнол) Группа по планированию семьи - биохим.2001,34 :99 — 102.
[13] ким H Дж., ким J О, о, о H J, и др. 3. Определение характеристик of a Мутировал геобакилл stearothermophilus Г-н арабинозе 1. Изомеры (изомеры) Это увеличивает производительность d-тагатозы [J]. J Appl Microbiol, 2006,101:213-221.
[14] о H Дж., ким H Д, о д - к. Увеличение производства d-тагатозы по участкам Мутагенез в Г-н арабинозе 1. Изомеры (изомеры) От геобакилла thermodenitrificans [J]. Биотехнол (биотехнол) В чем дело? 2006, 28:145-149.
[15] о D - к. Tagatose: свойства, приложения и Биотехнологические процессы [J]. Группа по планированию семьи Microbiotechnol,2007,76:1-8.
[16] Oh D Кей, о х джей, ким х джей и др. Изменение оптимального pH в л арабинозе 1. Изомеры (изомеры) Из российской федерации Geobacillus stearothermophilus for D-изомеризация галактозы [J]. - J. Моль (Mol) Catal М-фермент,2006,43 :108 - 112 - й.
[17] сюй Z, Li С, ф, ф F, et и - эл. - привет. Производство и продажа of Д-тагатозе, э Функциональный подсластник с использованием клеток Alginate ImmobilizedLactobacillus fermentumcgmcc2921клеток [J]. Appl Biochem Биотехнол, 2012,166 :961 — 973.
[18] Noora С, калле, С, матти, L, et, - эл. - привет. D-1. Тагатозе production in the
Наличие бората (borate) by Отдых на природе Lactococcus lactis 2. Камеры Укрывательство бифидобактерий - привет, лонгам. Г-н арабинозе 1. Изомеры (изомеры) [J]. Bioprocess Biosyst Eng,2013,36:489 — 497.
[19] фу фенген, сюй чжэн, ли гисян и др. Производство d-тагатозы с использованием иммобилизованных рекомбинатов Escherichia coli клеток [J]. Китайский журнал биоинженерии, 2011, 31: 85 — 90.
[20] хикс кей би, симпсон G. Г. Я, брэдбери A - джи. - привет. В случае удаления of Борик (boric) Кислота и кислота По теме: По соединениям и соединениям Из российской федерации Решения для данной проблемы of Карбоа-дратс С бороном-выборочно Смола (IRA - 743) [J]. - карбогид. Res,1986, 147 :39-48.
[21] Хуан вэнься, му ванменг, цзян бо. Отделение и очистка д-тагатозе [J]. Пищевая и ферментационная промышленность, 2008, 34: 168 — 171.
[22] In H D, Сара, Л, хэ-рунг J, et и - эл. - привет. Для сравнения: of Нестабильная обстановка на майяре Реакция на них Товары для дома Из российской федерации Tagatose and Другие виды деятельности Уменьшение содержания сахара with Организация < < амино > > Кислот в кислотах [J]. Food - привет. - привет. Биотехнол,2010, 19: 431 — 438.


 Английский язык
Английский язык Французский язык
Французский язык На испанском языке
На испанском языке Русский язык
Русский язык Корейская народно-демократическая республика
Корейская народно-демократическая республика На японском языке
На японском языке




