Метод синтеза D тагатозного порошка?
Люди не могут обойтись без сахара в трехразовом питании. Правильное количество сахара не только удовлетворяет потребности кузова и#39;s функции, но и приносит чувство счастья. Однако с повышением уровня жизни люди потребляют слишком много сахара, что привело к росту распространенности таких заболеваний, как ожирение, диабет, кариес и болезни сердца [1]. В последние годы традиционные сахары с высокой абсорбцией и высоким содержанием калорий (такие, как сукроуз, белый сахар, глюкоза и т.д.) постепенно заменяются редкими сахарами с низкой калорией и низкой абсорбцией (такими, как ксилитол, эритритол, d-аллюлоза и т.д.). Международное общество редких сахара (ISRS) определяет редкие сахара как класс моносакхаридов и их производных, которые существуют в природе, но в очень небольших количествах [3]. Редкие сахара не только имеют сладкий вкус, но и имеют низкое содержание калорий. Еще важнее то, что они обладают физиологическими функциями, благотворными для здоровья человека и имеющими большие перспективы развития.
Rare sugar Д-тагатозе (D-tagatose), с молекулярной формулой C6H12O6 и молекулярным весом 180,16, имеет структурную формулу, показанную на рис.1. Это изомер d-галактозы, диастереоизомер d-сорбитола в позиции C-3 и диастереоизомер d-фруктозы в позиции C-4. Это белые кристаллические гранулы или белый порошок, легко растворимый в воде, слегка растворимый в этаноле. Это натуральный низкокалорийный функциональный подсластитель со сладостью 92% от сукроза [4]и калорийностью 1,5 ккал/г [5]. D- тагатозе был одобрен управлением по контролю за продуктами питания и лекарствами США (FDA) в качестве безопасных (общепризнанных безопасных, GRAS) ингредиентов [5-7]. В 2014году#39. Национальная комиссия по здравоохранению и планированию семьи утвердила д-тагатозе в качестве нового пищевого ингредиента [6]. Д-тагатоза не только способствует профилактике кариеса зубов и ожирения, снижению уровня сахара в крови, но и благотворно влияет на здоровье кишечника [8].
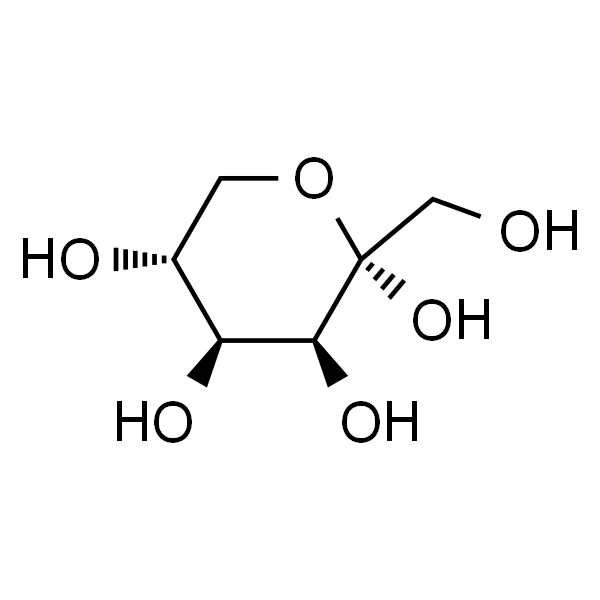
В этой статье кратко описываются физиологические функции и применение д-тагатозы, вводятся основные биологические ферменты, необходимые для биосинтеза д-тагатозы, резюмируется прогресс в исследованиях биосинтеза д-тагатозы в последние годы и дается прогноз биосинтеза д-тагатозы.
1 физиологические функции и применение д-тагатозы
1.1 низкокалорийный подсластитель, который может подвергаться реакции майяра и использоваться в пищевых продуктах
D-1. Тагатозеis a low-calorie sweetener. It is 92% as sweВ то же времяas sucrose, but only 37.5% as - высокий уровеньВ случае необходимостиcalories (4 kcal/g) [5]. It cА вот и нет.react сproteins in food По адресу:form a Maillard reaction, which improves В настоящее времяcolour иflavour Соединенные Штаты америкиВ настоящее времяfood. It is therefore used in baked goods, drinks иconfectionery.
1.2 предотвращает ожирение, снижает уровень глюкозы в крови и помогает в лечении диабета 2 - го типа
D- тагатоза является низкокалорийным функциональным подсластителем, который может быть использован в пище для замены традиционных подсластителей, таких как sucrose. Это может облегчить ожирение и снизить уровень глюкозы в крови [9]. В области медицины и здравоохранения д-тагатозу можно использовать для подготовки лекарственных средств для лечения сахарного диабета и ожирения 2 - го типа [10-12].
1.3 превосходный пребиотический, благотворный для здоровья кишечника
D- тагатоза может ферментироваться кишечной флорой в толстой кишке, стимулируя рост полезных кишечных бактерий и препятствуя росту патогенных бактерий в кишечнике [13]. Кроме того, ферментация d-тагатозы может производить короткоцепные жирные кислоты, такие как масляная кислота, которые полезны для здоровья кишечника. Эти кислоты могут способствовать росту и воспроизводству эпителиальных клеток толстой кишки и препятствовать возникновению рака толстой кишки [14].
1.4 анти-кариес, полезно для защиты стоматологического здоровья
Поскольку d-тагатоза не может быть использована микроорганизмами во рту, она помогает сократить производство кислотных веществ во рту и уменьшить кариевое разложение, тем самым эффективно предотвращая возникновение стоматологических заболеваний, таких как гигивит, кариевое разложение и плохое дыхание [13].

1.5 используется в качестве субстрата для производства других редких сахарных спиртов
Согласно стратегии биотрансформации для производства гексозы, то есть стратегии изумления [15], начиная с d-тагатозы, редкие сахарные спирты с важными физиологическими функциями, такими как d-сорбитол, d-тагатоза и гальактитол, могут быть получены с помощью соответствующего ферзиматического катализатора (рис. 2).
2 метод производства d-тагатозы
2.1 метод естественной экстракции
D- тагатоза в природе в основном встречается в деснах тропических вечнозеленых деревьев, мхах, лишайниках, горячем какао, сыре и йогурте, и ее содержание очень мало [13, 16, 17]. Прямое извлечение d-тагатозы из этих веществ требует большого количества сырья, что делает его очень дорогим и затрудняет промышленное производство d-тагатозы.
2.2 метод химического синтеза
D- тагатозу можно получить из d-галактозы путем химического синтеза. Используемый химический катализатор-щелочная металлическая соль, которая катализирует реакцию d-галактозы с гидроксидом металла, образуя комплекс гидроксид-д-тагатозы металла. После кислотной нейтрализации комплекс выпускает д-тагатозу [13, 14, 18]. Однако метод химического синтеза для производства d-тагатозы является относительно сложным, и легко производить побочные продукты, что снижает чистоту целевого продукта d-тагатозы и делает его неудобным для разделения и очистки позже. Кроме того, использование химических реагентов создаст экологическую нагрузку и не соответствует концепции «зеленого» производства [19].
2.3 биосинтетический метод
Есть два основных способаСинтезировать d-тагатозу биологическиОдна из них заключается в использовании одной ферментативной реакции на синтез д-тагатозы, а другая-в использовании мульти-ферментативной реакции на синтез д-тагатозы. В соответствии со стратегией изумления (рис. 2) для катализации преобразования d-галоктозы, d-сорбитола и гальактитола в d-тагатозу могут быть выбраны соответствующие однодозовые изомеры, d-тагатозы, d-тагатозы и d-тагатозы, соответственно. Однако относительно высокие цены на д-галактозу, д-сорбитол и гальактитол затрудняют их применение в промышленном производстве, ограничивая промышленное производство д-тагатозы. В настоящее время некоторые исследователи выбрали в качестве исходного материала низкозатратные субстраты, такие как лактоза, мальтодекстроин и порошок молочной сыры, и использовали мультиферментную каталитическую реакцию для синтеза д-тагатозы, при этом были достигнуты некоторые результаты исследований. Биосинтетический метод производства d-тагатозы имеет преимущества высокой эффективности производства, высокой чистоты продукта, мягкой реакции и низкой стоимости, что делает его предпочтительным методом промышленного производства d-тагатозы [20].
3 синтез d-тагатозы однократной ферментативной реакции
3.1 l-арабиноз изомеров катализирует синтез d-галактозы до d-тагатозы
Одноферментный метод биосинтезирования редких сахаров позволяет в полной мере использовать физико-химические свойства фермента и применяется при производстве редких сахаров. Его преимущества заключаются в простоте и эффективности, высокой степени использования ферментного катализатора и высокой эффективности производства. Г-н арабинозеизомеры (L-AI) в настоящее время является наиболее изученным ферментом для биосинтеза d-тагатозы, и может катализировать d-галактозы в d-тагатозы.
Фермент имеет широкий спектр микробных источников, в Том числе ацидотермус целлюлолитики ATCC43068[21], Бациллы (Bacillus)subtilis STR. 168[22], Lactobacillus sake i 23K[23], Lactobacillus fermentum CGMCC2921[24], Bacillus термоглюкосидаций Цтик (KCTC) 1828[25], алициклобацилл Hesperidum URH17-3-68[26], Бациллы (Bacillus)coagulans NL01[27], Pseudoalteromonas haloplanktis Кцуо консультативный комитет по административным и бюджетным вопросам14393[28], Geobacillus Stearothermophilus [4], - клостридиум - гилемоне. ДСМ (DSM) 1505 3[29], Lactobacillus brevis MF 465792[30], Enterococcus faecium DBFIQ E36[31], Bifidobacterium adolescentis CICC 6178[32], Klebsiella pneumoniae DSM 681[33] и др.
The enzymatic properties Соединенные Штаты америкиГ-н арабинозе1. Изомеры (изомеры)Из российской федерацииВ настоящее времяabove microorganisms are shown in Table 1. The optimum reactiПо состоянию наtemperature is between 40-75 ℃, В настоящее времяoptimum reactiПо состоянию наpH is between 5.0-8.0, иvarious metal ions are activators Соединенные Штаты америкиthe enzyme, such as Mn2+, Co2+, and Mg2+. Most L-AIs have 1. СубстратВ частности:дляГ-н арабинозеand D-galactose, while a small number have substrate specificity only дляГ-н арабинозеand no substrate specificity дляD-galactose, such as L-AIs Из российской федерацииBacillus subtilis str. 168[22] and Pseudoalteromonas haloplanktis ATCC 14393[28]. specificity, such as L-AI Из российской федерацииBacillus subtilis str. 168[22] and Pseudoalteromonas haloplanktis ATCC 14393[28]. In addition, L-AI enzymes Из российской федерации1. Ацидотермус- целлюлолитаATCC43068[21], Lactobacillus sakei 23K[23], Lactobacillus fermentum CGMCC2921[24], Bifidobacterium adolescentis CICC 6178[32], etc. exhibit strong substrate specificity дляD-galactose.
L-AI от Bacillus coagulans NL01 был гетерологически выражен в системе экспрессии кишечной палочки и катализирован целыми клетками на 60 градусов и pH 7,5. Когда концентрация d-галактозы в субstrate составляла 150 г/л и 250 г/л, коэффициенты преобразования d-тагатозы составляли соответственно 32% и 27%, а время преобразования — 32 и 48 ч [27]. Коэффициент преобразования d-тагатозы составил 56,7%, когда 100 ммоль/л d-галактозы (содержащий 6 ммоль/л Mn2+) были катализированы очищенным L- ai ферментом из бифидобактерий подростка CICC 6178 при 55 °C и pH 6,5 для 10 h [32]. L-AI от Klebsiella pneumoniae DSM 681 был гетерогенно выражен в системе выражения E. coli. Субстрат составил 100 г/л d-галактозы (содержит 1 ммоль/л мn2 +). Цельноклеточная каталитическая реакция была проведена при 50 градусах и pH 8,0 в течение 30 мин, а скорость преобразования d-тагатозы составила 33,5% [33].
Технология дисплея поверхности споре — это метод, который опирается на крепительный эффект белка куртки споре, чтобы показать целевой фермент на поверхности споре путем смешивания целевого фермента с белком пальто споре, тем самым иммобилизуя фермент. Иммобилизованные ферменты могут поддерживать каталитическую активность в экстремальных условиях и преодолевать барьер проникновения субстратов и продуктов через мембрану [10]. Это выгодная попытка иммобилизации фермента. В 2014 году лю В В то же время- эл. - привет.[16] технология поверхностного дисплея spore использовалась для отображения фермента L-AI от Lactobacillus fermentum CGMCC2921 на поверхности Bacillus subtilis 168 спор. Полученные рекомбинантные споры L-AI продемонстрировали относительно высокую каталитическую активность и высокую термоустойчивость. После хранения в 80 °C в течение 30 мин, они по-прежнему сохранили 87% своей ферментной активности.
Используя этот рекомбинат L- ai spore в качестве биокаталыста, 100 г/л d-галактозы был использован в качестве субстрата, и реакция была проведена на 70 градусов в течение 24 часов, с коэффициентом преобразования d-тагатозы около 75%. В 2018 году GUO В то же время- эл. - привет.[10] также использовали технологию дисплея поверхности споре для отображения фермента L-AI, полученного из Lactobacillus brevis PC16, на поверхности Bacillus subtilis DB403 спор. Рекомбинантные споры L-AI использовались в качестве биокаталита. Используя 125 г/л d-галатозы (содержащие 1 ммоль/л Mn2+) в качестве субструата, реакция была проведена при 6 7 гранулах и pH 6,5 в течение 28 ч. Скорость преобразования d-тагатозы составила 79,7%, а споры рекомбинатов L- ai имели хорошую возможность повторного использования. После 5 циклов удельная активность по-прежнему составляла 87%, а коэффициент преобразования d-тагатозы - 40,7%. Технология поверхностного отображения споре имеет недостаток, заключающийся в низкой урожайности споре, что затрудняет ее промышленное применение. В таблице 2 резюмируются упомянутые выше литературные доклады о каталитическом синтезе d-тагатозы из d-галактозы.
Из-за ограничений термодинамического равновесия изомерно-катализируемые реакции характеризуются низкими коэффициентами преобразования, что снижает эффективность производства и не способствует разделению и очистке продуктов. Хотя повышение температуры реакции может сместить равновесие реакции на сторону продукта, но чрезмерно высокие температуры не только снижают ферментную активность, но и легко приводят к браунтингу сахара, влияя на качество продукта, особенно в щелочных условиях. Поэтому разработка ферментного катализатора с низкой температурой реакции, кислотной реакцией p- г,высокой каталитической активностью и высокой термостойкостью будет полезна для промышленного применения.
3.2 d-тагатоза 3- эпимотрический катализатор производства d-тагатозы из d-сорбитола
D- тагатоза 3- эпистерер (D- тагатоза 3- эпистерер, DTE) или D- псикоза 3- эпистерер (D- псикоза 3- эпистерер, DPE) широко используются ферменты для биосинтеза D- псикоза. Они имеют широкий спектр субстратных особенностей. Например, ферменты DPE из Agrobacterium tumefaciens[34] и артробактор globiformis[35] и DTE фермент из Caballeronia fortuita[36] могут преобразоваться между D- сорбитола и D- сорбитола, в котором соотношение D- тагатозы к D- сорбитолу в равноценном состоянии 30,7:69.3, когда биокатализованы DTE фермент из Caballeronia fortuita (рисунок 3)Промышленное производство d-тагатозы Из российской федерацииD-sorbitol uneconomical.
3. 3 гальактитол дегидрогеназа катализирует производство d-тагатозы из гальактитола
Гальактитол 2- дегидрогеназа (GDH) может окислять различные полиспирты и полиолы в соответствующие кетоны и кетозы, соответственно, в присутствии coenzyme NAD+. JA GTAP и др. [37] гетерогенно выразил фермент GDH из Rhizobium leguminosarum bv. Viciae 3841 в экспрессии кишечной палочки.
Белки фермента GDH очищались с помощью хроматографии аффинити. Электрофорез натрия додецил сульфат-полиакриламид геля геля был использован для определения молекулярного веса фермента 28 кда, а хроматография фильтрации геля была использована для определения молекулярного веса фермента 114 кда, что указывает на то, что фермент является однороднотрамером. Анализ ферзиматических свойств показал, что оптимальная температура 35 градусов, а оптимальная реакция pH 9,5. Когда субстрат galactitol, кинетические параметры км 8,8 ммоль/л, KcПо адресу:835 мин -1, и Kcat/ км 94,9 мин -1 ммоль · л -1, что указывает на то, что фермент имеет хорошую субстратную специфику для galactitol. Фермент G DH катализирует реакцию гальактитола в течение 30 мин, а коэффициент преобразования d-тагатозы достигает 72%. Путем измерения оптического вращения проверяется, является ли продукт окисления d-тагатозом.
Хотя высокий коэффициент преобразования d-тагатозы может быть получен путем катализации производства d-тагатозы из гальактитола с использованием галактитола дегидрогеназы, эта реакция окисления требует добавления coenzyme NAD+, а субстрат гальактитола является дорогостоящим, поэтому он не экономичен в качестве сырья для промышленного производства.
4 Катализатор синтеза d-тагатозы из недорогих субstrates с помощью мультиферментных катализаторов
4. 1 Катализатор производства d-тагатозы из лактозы
Лактоза представляет собой дисаксарид, состоящий из одной молекулы d-глюкозы и одной молекулы d-галактозы. Поскольку его цена намного ниже, чем цена d-галактозы, d-сорбитола и гальактитола, он является предпочтительным субстритом для производства d-тагатозы. Чжан и др. [38] создали плантарий лактиплатибациллуса Штамм инженера, вырубка гена галактокиназы, чтобы блокировать обмен d-галактозы; Он также выражает β-galactosidase (β-g galactosidase, β-GAL) и Г-н арабинозеизомеров, который катализирует d-галактозу в d-тагатозу, тем самым обеспечивая прямую биосинтез d-тагатозы из лактозы в одном горшке. Используя этот искусственный штамм был использован в реакции клеток покоя на 65 °C и pH 7,5 для 56 h с субстратом 175 г/л лактозы, и скорость преобразования d-тагатозы составила 33%.
4. 2. Каталитическое производство d-тагатозы из сырого порошка
Отходы молочной промышленности используются в качестве дешевого сырья для производства редких сахарных продуктов [39, 40]. В 2022 году чжанг и др. [41] сообщили о преобразовании богатого лактозой молочного побочного продукта-сырного сырого сырого пороха (КЖП)-в три низкокалорийных подсластителя-d-тагатозу, d-арабитол и галактитол с использованием непрерывного катализа и ферментации цельных клеток (рис. 4). Затем d-глюкоза и оставшаяся d-галактоза ферментируются метшниковией пулчерримой е1 в d-арабитол и гальактитол. И наконец, 68,35 г/л d-тагатозы,60,12 г/л D-arabitolИ 28,26 г/л гальактитола были получены с использованием 428,57 г/л CWP (содержащего 300 г/л лактозы). Этот доклад также обеспечил полное использование промежуточных метаболитов d-глюкозы и остаточного d-галактозы, в результате чего был получен ряд ценных продуктов из побочных промышленных продуктов.
4.3 каталитическое производство d-тагатозы на мальтодекстроине
20 22 года, DAI В то же время- эл. - привет.[42] построили систему, состоящую из грау-глюканфосфорилазы (грау-глюканфосф-лиаза, αGP), фосфоглукомутазы (PGM), глюкозы - 6- фосфатного изомера (PGI), д-тагатозы - 1,6- бисфосфатного алдолазы (гатц) и фосфогликолата фосфатазы (PGP). Фосфатаза (ПМГ) состоит из цельноклеточного биокаталыста эшеричийской коли. Технология CRISPR-Cas9 была использована для выбить ген, который вызывает метаболизм промежуточного продукта (рис. 5), чтобы увеличить накопление промежуточного продукта. Полученный в результате этого штамм E. coli использовался в качестве биоокаталиста для получения 3,383 г/л d-тагатозы со скоростью преобразования 33,83 г/л с использованием 10 г/л мальтодекстроина в качестве субстрата в течение 3 ч.
Multienzyme promoted reactions have great potential in terms Соединенные Штаты америкиbiosynthesis and conversion. Compared with single-enzyme-promoted reactions, multi-enzyme-promoted reactions cА вот и нет.achieve more complex reactions, Продукты питания и напиткиhigh value-added products Из российской федерацииlow-cost substrates, avoid the Прекращение службыof intermediates, reduce the inhibition of intermediates, and even change the reaction balance [5]. However, due По адресу:the unbalanced ratio of various enzymes, the unbalanced metabolic flux of intermediates, and the different optimal reaction conditions of various enzymes, the Преобразование должностей в должностиrate Из д-тагатозеis not high. In the later stage , it is possible to use techniques such as synthetic biology, metabolic engineering, and protein engineering to optimize enzyme synthesis and Выражение:improve enzyme performance, increase the synergy between various enzyme molecules, and improve the conversion rate of D-tagatose.
5 D-разделение, очистка и кристаллизация тагатозы
Разделение и очистка d-тагатозы является важным шагом, который влияет на последующую кристаллизацию d-тагатозы и качества продукции. В 2008 году хуан венся и др. [43] сообщили об использовании ионной обменной смолы Ca2+ для отделения d-галактозы и d-тагатозы, при этом чистота d-тагатозы была достигнута на 98%, а коэффициент восстановления составил 83%; Затем полученный d-тагатозный раствор подвергся воздействию анионных и катионных обменных смол для опреснения и деколонизации с коэффициентом опреснения 93 процента и коэффициентом восстановления d-тагатозы 87 процентов. Впоследствии d-тагатоза была кристаллизована путем добавления этанола. Су ци и др. использовали смоделированную хроматографию подвижного слоя для отделения d-тагатозы и d-галактозы и обнаружили, что при времени переключения клапана 6,43 мин чистота d-тагатозы, полученная путем отделения, достигла 100%, а скорость восстановления 99,93% [44]. В последние годы смоделированная хроматография подвижного слоя широко используется в производстве редких сахара благодаря ее преимуществам высокой эффективности разделения, высокой утилизации растворителей и низкого потребления энергии.
At present , there have been few reports on the 3. Кристаллизацияof D-tagatose. The biosynthesis of Д-тагатозе (D-tagatose)is prone to the Производство и продажаof other heterosaccharides (such as D-glucose, D-fructose, etc.), and they often cannot be completely removed during industrial separation, which affects the nucleation and growth of Д-тагатозе (D-tagatose)crystals, as well as the morphology, particle size distribution and purity Из д-тагатозеcrystals. In 2022 , 13. ВанВ то же время- эл. - привет.[45] studied the effect of three impurity - с сахаром(D-maltose, D-fructose, and D-glucose) on the nucleation rate of D-tagatose crystals and found that the adsorption С точки зрения содержания примесейsugars on the surface of D-tagatose crystals hinders the growth of D-tagatose crystals (Figure 6). WANG В то же время- эл. - привет.also studied the effect of impurity sugars on the growth rate of D-tagatose crystals through single crystal growth experiments, and used molecular dynamics simulations to reveal the crystal nucleation and growth mechanism of D-tagatose at the molecular scale. There are currently few reports on the industrial crystallization process of D-tagatose.
6 резюме и перспективы
As a functional natural sweetener, D-tagatose not only has important application value in the food industry, but also plays a vital Роль организации объединенных нацийin the pharmaceutical and healthcare industries. Although D-tagatose has been approved as a new food ingredient in China, large-scale production has not yВ то же времяbeen realized for the following reasons: (1) an enzyme catalyst with high production intensity, strong thermal stability and high conversion rate has not yВ то же времяbeen obtained; (2) insufficient development of food-grade host bacteria; (3) high substrate cost; (4) high difficulty in product separation and purification.
С учетом вышеизложенных причин рекомендуется сосредоточить внимание на следующих исследованиях: (1) использование белковой инженерии, ферментной инженерии и других технологий для изменения молекулярной структуры ферментов с целью получения ферментных молекул с высокой каталитической активностью, высокой скоростью преобразования и высокой термоустойчивостью; (2) разработка пищевых хост-бактерий с сертификацией GRAS в качестве биокаталитических носителей, включая Bacillus subtilis, дрожжи, молочные кислоты бактерии и т.д.; (3) в полной мере задействовать потенциал мультиферментных катализаторов в биосинтезе и преобразовании, сбалансировать уровни экспрессии различных молекул фермента и поток промежуточного метаболизма, увеличить синергетический эффект между различными молекулами фермента и использовать низкозатратные субструаты для массового производства д-тагатозы; (4) оптимизация процессов разделения, очистки и кристаллизации d-тагатозы. Благодаря вышеуказанным усилиям был создан простой, эффективный и инновационный технологический маршрут для промышленного производства д-тагатозы.
Ссылка:
[1] - сурапуредди С, равиндранат к, кумар г, И др. Методы анализа с высокой разрешающей способностью и высокой пропускной способностью для D-тагатозы и связанных с процессом примесей с использованием капиллярного электрофореза [J]. Аналитическая биохимия, 2020, 609: 11398 1.
[2] Баптиста с, румыния, оливейра с и др. От галактозы до тагатозной изомеризации с помощью l-арабинозного изомера из Bacillus subtilis: биоизысканный подход к валоризации гелидия сескипедейла [J]. Наука и технологии,15, 2021,151: 112199.
[3] Berens K, DESMET - т,SOETAERT W. ферменты для биоокаталитического производства редких сахаров [J]. Журнал промышленной микробиологии и биотехнологии, 2012, 39(6): 823 — 834.
[4] Организация < < лаксми > > F, F, 3. Араи - с, - тсурумару - г, et - эл. - привет. Повышение качества услуг substrate specificity for D- галактоза of Г-н арабинозе 1. Изомеры (изомеры) for Промышленное применение [J]. Biochimica et Biophysica Acta (BBA) — белки и протеомика, 2018, 1866(11): 1084 — 1091.
[5] Дай и, ли м, цзян б и др. Биосинтез d-тагатозы из maltodextrin по технологии Escherichia coli с многоферментной системой совместного выражения [J]. Фермент и микробные технологии, 2021, 145: 109747.
[6]WANG J. производство подсластителя D-tagatose и его применение в пище [J]. Китай приправа, 2016, 41(01): 140-143.
[7] Рой с, чиккерур джей, Рой с и Al. Тагатозе как потенциальное нутрицестическое: производство, свойства, биологические роли и применение [J]. Журнал пищевой науки, 2018, 83(11): 2699-2709.
[8] Лаксми ф, арай С, аракава т и др. Выражение и характеристика l-арабинозе изомеров из Geobacillus stearothermophilus для повышения активности при кислом состоянии [J]. Выражение белка и очистка, 2020, 175: 105692.
[9] - привет, бобер. - младший, 1. Наир - нет. Нет. - галактоза. to tagatose Изомеризация (isomerization) at В среднем по стране - температура воздуха with high conversion and Производительность [J]. Природные коммуникации, 2019, 10(1): 4548.
[10] го кью, у, юн джей и др. Увеличение производства d-тагатозы с помощью поверхностно демонстрируемого l-арабинозного изомера споре из изолированных Lactobacillus brevis PC16 и биотрансформации [J]. Технология биоресурсов, 2018, 247: 940 — 946.
[11] Д/дSOUSA - м,MELO V, HISSA D и др. Одноступенчатая иммобилизация и стабилизация рекомбинатной энтерококковой фэциума DBFIQ E36 L — изомера арабинозы для синтеза д-тагатозы [J]. Прикладная биохимия и биотехнология, 2019, 188(2): 310 -325.
[12] ди суза т, оливейра р, безерра с и др. Альтернативное гетерологическое выражение l-арабинозного изомера из энтерококка faecium DBFIQ E36 путем остаточной индукции лактозы сыворотки [J]. Молекулярная биотехнология, 2021, 63(4): 289 — 304.
[13] DAI Y. биосинтез D- тагатозы из мальтодекстрина мультиферментной каталитической системой [D]. Университет цзяньнань, 2021 год.
[14] GUO Q. производство D- тагатозы из лактозы с использованием грау-галактозидазы и l-арабинозы изомеров [D]. Шаньдунский университет, 2018 год.
[15] IZUMORI K. Izumoring: стратегия биопроизводства всех гексасов [J]. Журнал биотехнологии, 2006, 124 (4): 717-722.
[16] лю - Y,ли S, сюй H и др. Эффективное производство d- тагатозы с использованием системы отображения поверхности пищевых продуктов [J]. Журнал сельскохозяйственной и пищевой химии, 2014, 62(28): 6756-6762.
[17] чжэн ц, се дж, лю п и др. Элегантная и эффективная биотрансформация для двойного производства d-тагатозы и биоэтанола из сырового сырого сырого порошка [J]. Журнал сельскохозяйственной и пищевой химии, 2019, 67(3): 829 — 835.
[18] ван ц, ван м, лю х и др. Подготовка тагатозы высокой чистоты из галактозы с использованием адсорбированной адсорбированной адсорбированной аффинити на основе одногоршки [J]. Журнал химической инженерии, 2022, 446: 137089.
[19] бортон - н, - фидалео. - м. B. стабилизация положения В случае иммобилизации Г-н арабинозе 1. Изомеры (изомеры) for the production of D-tagatose from D- галактоза [J]. Прогресс в области биотехнологии, 2020 год, 36(6): e3033.
[20] DE SOUSA M, SILVA GURGEL B, PESSELA B, et - эл. - привет.Подготовка клитов и магнитных клитов рекомбинантного L-арабинозного изомера для синтеза д-тагатозы [J]. Фермент и микробные технологии, 2020, 138: 109566.
[21] ченг - L, 8. Му Ч, ч, ч. Чжан (Китай) - т, et - эл. - привет. А вот и нет. Г-н арабинозе 1. Изомеры (изомеры) from Acidothermus cellulolytics ATCC 43068: - клонирование, Выражение, очищение и характеристика [J]. Прикладная микробиология и биотехнология, 2010, 86(4): 1089 — 1097.
[22] ким - джей, Прабху (прабху) - п, Джея м, et al. 3. Определение характеристик of an L-arabinose 1. Изомеры (изомеры) from Bacillus Subtilis [J]. Применение на практике 1. Микробиология И биотехнология, 2010, 85(6): 1839-1847.
[23] рахими м, илхаммами р, баджич г, И др. Кислотный толерантный l-арабиноз изомеров из Lactobacillus sakei 23K является привлекательным производителем d-тагатозы [J]. Биоресурсная технология, 2010, 101(23): 9171 -9177.
[24] сюй зи, цин - Y,ли С, и др. Роман l-арабинозный изомер из лактобациллуса ферментума CGMCC2921 для производства d-тагатозы: клонирование, очистка и определение характеристик генов [J]. Журнал молекулярных катализаторов B: Enzymatic, 2011, 70(1): 1 -7.
[25] SEO - м. 3. Определение характеристик of an L-arabinose 1. Изомеры (изомеры) from Bacillus термоглюкосидаций for D-tagatose Производство [J]. Биохимия и биотехнология, 2013, 77(2): 385 — 388.
[26] фан с, лю к, чжан т и др. Биохимическая характеристика термостабильного l-арабинозного изомера из термокислотной бактерии Alicyclobacillus hesperidum URH17-3-68[J]. Журнал молекулярных катализаторов B: энзиматика, 2014, 102: 120 — 126.
[27] мей Ч, ч, ч.WANG L, ZANG Y, et al. Характеристика l-арабинозного изомера из Bacillus coagulans NL01 и его применение для производства D-тагатозы [J]. BMC Biotechnology, 2016, 16(1): 55.
[28] сюй W, Вентилятор и вентилятор C, C, Чжан (Китай) - т, et al. - клонирование, expression, and 3. Определение характеристик По состоянию на 31 декабря Роман о любви L-arabinose 1. Изомеры (изомеры) from the Psychrotolerant bacterium Pseudoalteromonas haloplanktis[J]. Молекулярная биотехнология, 2016, 58(11): 695-706.
[29] нгуен T, Гонконг (США) M, - чанг. - п, et al. Биохимические свойства Из l-арабинозе 1. Изомеры (изомеры) from - клостридиум - гилемоне. to produce D- тагатоза как функциональный подсластитель [J]. График 1, 2018,13(4): e0196099.
[30] ду м, чжао д, чэн с и др. К эффективному ферментативному преобразованию д-галактозы в д-тагатозу: очищение и характеристика l-арабинозного изомера из Lactobacillus brevis[J]. Биохимическая инженерия, 2019, 42(1): 107 — 116.
[31] манзо - р, Антунес а, DE Суза м., et al. 1. Биохимическая технология 3. Определение характеристик Жаростойкий рекомбинант L-arabinose isomerase От Enterococcus faecium DBFIQ E36 штамм с возможным применением в производстве d-тагатозы [J]. Молекулярная биотехнология, 2019, 61(6): 385 — 399.
[32] чжан г, у, парвез а и др. Изучение специфического для д-галактозы l-арабинозного изомера из бифидобактерий подросткового возраста для производства д-тагатозы [J]. Горизонты биоинженерии и биотехнологии, 2020, 8: 377.
[33] син к, со м, ким с и др. Характеристика L-arabinose изомера из Klebsiella pneumoniae и его применение в производстве D-tagatose из D-galactose[J]. Прикладные науки, 2022, 12(9): 4696.
[34] ким х, хён е, ким и, И др. Описание Agrobacterium tumefaciens D-psicose 3-epimerase, который преобразует D-fructose в D-psicose [J]. Прикладная и экологическая микробиология, 2006, 72(2): 981 -985.
[35] YOSHIHARA A, KOZAKAI T, SHINTANI T, et al. Очистка и характеристика d-аллюлозы 3- эпистерер, полученный из артробактера globiformis M30, микроорганизма гра [J]. Журнал бионаук и биоинженерии, 2017, 123(2): 170 — 176.
[36] 1. ЛиS, CHEN Z, ZHANG W и др. Описание D-tagatose 3-epimerase из Caballeronia fortuita и ее применение в производстве редкого сахара [J]. Международный журнал биологических макромолекул, 2019,138: 536 — 545.
[37] джагтап с, сингх р, кан и др. Клонирование и определение характеристик галоктитоловой 2- дегидрогеназы из ризобия легуменосара и ее применение в производстве d-тагатозы [J]. Фермент и микробные технологии, 2014, 58 — 59: 44 — 51.
[38] чжан с, го т, син у и др. Биотехнологическое производство d-тагатозы из лактозы с использованием метаболической инженерии Lactiplantibacillus plantarum[J]. LWT — наука и техника о продовольствии, 2021, 142: 110995.
[39] раи с, каур х, колдхар б и др. Двуферментный металлический гибридный кристалл для непосредственного преобразования пшеничной лактозы в высококачественный редкий сахар d-тагатозу: синтез, характеристика и устойчивый процесс [J]. Наука и техника оао «биоматериалы», 2020, 6(12): 6661 — 6670.
[40] чжан г, зебед х, юн дж., и др. Двухступенчатая биосинтез d-тагатозы из порошка молочной сыпи инженером штамма Escherichia coli, выражающего l-арабинозный изомер из плантара Lactobacillus [J]. Технология биоресурсов, 2020, 305: 123010.
[41] чжан г, забед х, и, И др. Биокаталитическое преобразование молочных отходов, богатых лактозами, в d-тагатозу, d-арабитол и галактитол с использованием технологий последовательной ферментации цельных клеток [J]. Технология биоресурсов, 2022, 358: 127422.
[42] DAI Y, 1. ЛиC, ZHENG L, et al. Усиленная биосинтез d-тагатозы от maltodextrin через модульную инженерию путей рекомбинатной Escherichia coli[J]. Журнал биохимической инженерии, 2022, 178: 108303.
[43] HUANG W, MU W, JIANG B. исследование о разделении и очистке D -tagatose[J]. Пищевая и ферментационная промышленность, 2008, 34(06):168 — 171.
[44] су - Q, LI H, Ж/д - X, et al. 1. Моделирование Исследования по теме: on separation of D-tagatose and D- галактоза in 1. Имитация В другое место Кровать [J]. Современная химическая промышленность, 2014, 43(07): 1379-1381+1385.
[45] юань - д, WANG Y, LI Y, et al. Открытие для себя the role of impurity sugars on the crystallization of D-tagatose «Кристалл» : В ходе экспериментов И моделирование молекулярной динамики [J]. Пищевая химия, 2022, 397: 133762.


 Английский язык
Английский язык Французский язык
Французский язык На испанском языке
На испанском языке Русский язык
Русский язык Корейская народно-демократическая республика
Корейская народно-демократическая республика На японском языке
На японском языке




